实验外包——一文带你了解活体成像技术
发布时间:2025-09-04
浏览次数:17587
作者:东极药物
小动物活体成像技术,是在1999年美国哈佛大学Weisslede提出的一项技术,该技术是指应用影像学方法, 对活体状态下的生物过程进行组织、细胞和分子水平的定性和定量研究。细胞在组织间的穿梭、分子间的相互作用、神经信···
小动物活体成像技术,是在1999年美国哈佛大学Weisslede提出的一项技术,该技术是指应用影像学方法, 对活体状态下的生物过程进行组织、细胞和分子水平的定性和定量研究。
细胞在组织间的穿梭、分子间的相互作用、神经信号的实时传递……这些曾经隐藏在“黑箱”中的生命奥秘,如今在活体成像技术下宛如一部部活生生的微观“电影”,能实时、动态、在原位观察生命如何在生物体内运作!
光学成像技术
生物发光成像(Bioluminescence Imaging)
原理:利用荧光素酶(Luciferase)基因标记目标细胞或基因,注射底物(如D-荧光素钠/钾盐)后,在氧和ATP存在下催化发光反应,光波长在540-600 nm,发光的强度与标记细胞的数目呈线性关系,可以分析动物体内特定的基因表达、细胞发育和相关生物学进程。
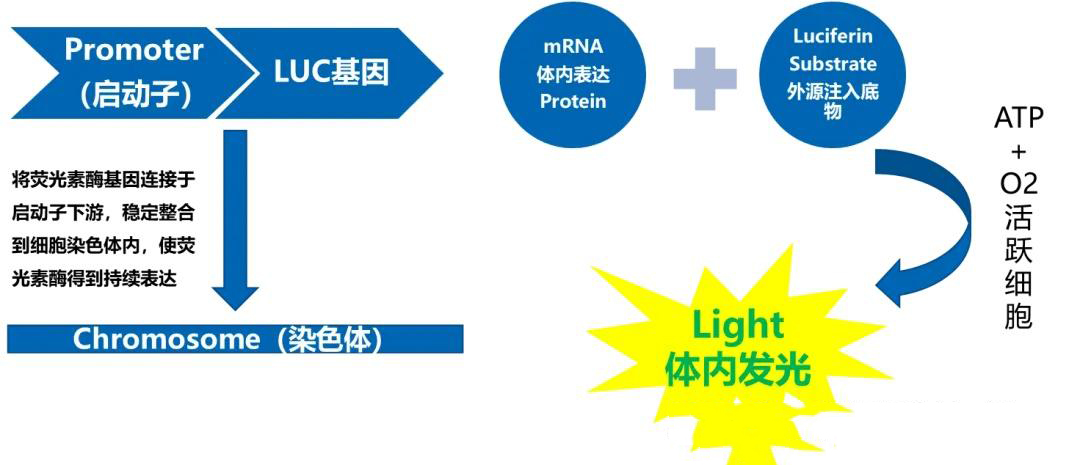
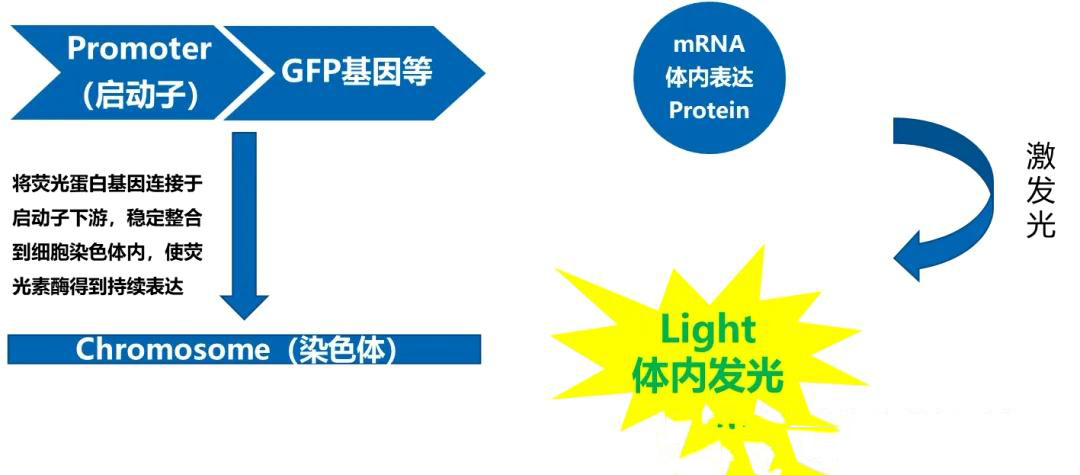
荧光成像(Fluorescence Imaging)
原理:通过荧光蛋白(如GFP、mCherry)或染料标记目标,经特定波长激发后发射荧光成像。
两大成像系统对比
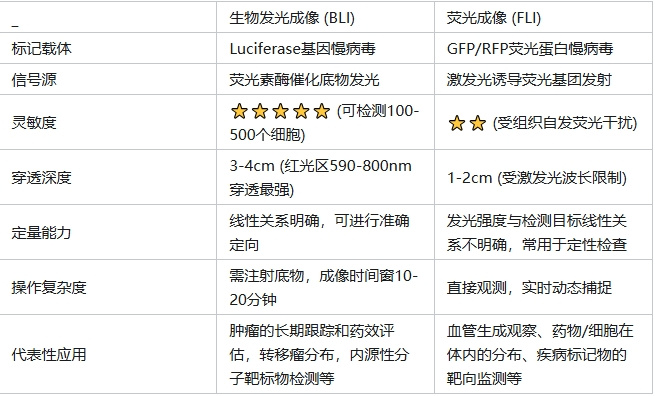
应用场景
一、肿瘤研究
1)肿瘤生长与转移示踪
将携带Luciferase和荧光蛋白基因的慢病毒感染肿瘤细胞(如胰腺癌、肝癌、乳腺癌细胞),构建稳转细胞系后接种至小鼠体内,通过生物发光成像实时监测原位瘤生长、远端转移(如肺转移、骨转移)及转移路径。
2)肿瘤特异性靶向成像
采用肿瘤特异性启动子(如端粒酶hTERT启动子)驱动报告基因表达,仅在端粒酶阳性的肿瘤细胞中激活荧光信号,实现高特异性成像,避免正常组织背景干扰。
3)肿瘤机制研究
结合基因编辑技术(如过表达/干扰特定基因),慢病毒双标记(Luciferase+目的基因)可同步观察基因功能与肿瘤表型变化。
二、干细胞治疗与再生医学
1)干细胞体内分布与存活监测
慢病毒转染干细胞(如脐带间充质干细胞)后表达Luciferase,注入动物模型皮下或静脉,通过活体成像追踪干细胞迁移、归巢及长期存活状态,评估治疗有效性。
2)干细胞治疗机制探索
在强直性脊柱炎等疾病模型中,标记的间充质干细胞可用于研究炎症微环境中的定向迁移机制。
三、药物研发与疗效评估
1)药效动力学研究
在移植瘤模型中,通过慢病毒标记的肿瘤细胞实时监测药物干预后肿瘤体积变化、转移抑制效果及复发情况。
2)药物靶向递送验证
结合报告基因与药物载体(如纳米颗粒),活体成像可直观显示药物在肿瘤部位的富集程度及代谢动力学。
从“看见”单根神经的超级CT,到让细胞发光的基因探针,活体成像技术正撕开生命暗箱!慢病毒载体的精准投递,赋予成像以时间维度与分子特异性。
文章出自:验外实包 想了解更多请关注:http://www.dj-cro.com/